向含有钙离子和镁离子的水或钻井液滤液中加入EDTA(或其盐)后,EDTA先与钙离子发生络合,其终点可用合适的指示剂确定。水或滤液的总硬度以钙离子浓度来表示,单位为毫克每升。如存在深颜色组分造成滴定重点难以分辨,可加入氧化剂(如次氯酸钠等),氧化这些组分予以解决。
mg/L
1. EDTA 溶液 (CAS No. 6381-92-6), 0.01 mol/L
2. 测钙离子用缓冲溶液:1 mol/L氢氧化钠(CAS No.1310-73-2)溶液
3. 钙指示剂:羟基蔡酚蓝(CAS No.63451-35-4)
4. 次氯酸钠(CAS No.7681-52-9)溶液:5.25%(质量分数)次氯酸钠的去离子水溶液
5. 乙酸(CAS No.64-19-7):冰醋酸
6. 去离子水或蒸馏水
7. 锥形瓶:150 mL
8. 移液管:5 mL 、10 mL
9. 移液管:1 mL、2 mL和5 mL
10. pH 试纸
11. 加热板
1. 用移液管取1 mL或更多样品于150 mL锥形瓶中。该样品体积将用于以下公式的计算。如滤液无色或颜色较浅,可省略2 - 5的步骤。
2. 用移液管加入10 mL次氯酸钠溶液并混合均匀。
3. 用移液管加入1 mL乙酸并混合均匀。
4. 将样品煮沸5 分钟,在煮沸期间按需加入去离子水以保持样品体积不变。煮沸可除去过量的氯气。将pH试纸浸在样品中可测试氯气是否除净。如试纸被漂白,则需要继续煮沸。充分煮沸过的 样品其pH值为5.0。
5. 冷却样品。
6. 用去离子水冲洗锥形瓶内壁并将样品稀释至约50 mL,加入10 mL〜15 mL测钙离子用缓冲 溶液或足量的NaOH,使pH值达到12 - 13。
注:可溶性铁离子可能会干扰终点的确定。如怀疑存在铁离子,可用三乙醇胺、四乙烯基戊胺和去离子水的混合液(体积比为1:1:2)作掩蔽剂。
7. 加入足量的钙指示剂(0.1 g〜0.2 g),如存在钙离子,则会呈现粉红色至酒红色。如指示剂加的过多,会导致终点不明显。
注:加入钙指示剂时如再加入几滴甲基橙指示剂,可使滴定终点较为明显。
8. 边摇动边用EDTA标准溶液滴定至终点,钙指示剂将由红色变为蓝色。继续加入EDTA溶液时不再有由红到蓝的颜色变化,即为最恰当的终点。
按公式计算钙离子含量Cca2+,单位为毫克每升。
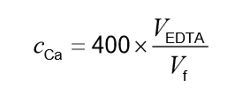
公式中:
Cca2+ - 钙离子含量,单位为毫克每升(mg/L);
VEDTA - 滴定中消耗的EDTA标准溶液体积,单位为毫升(mL)(1mL该浓度EDTA溶液中EDTA 的物质的量与1 mL 400 mg/L 钙离子的物质的量相同);
Vf - 滤液样品体积,单位为毫升(mL)。